顶级光动力治疗费用
光动力治疗的核心技术差异与费用关联
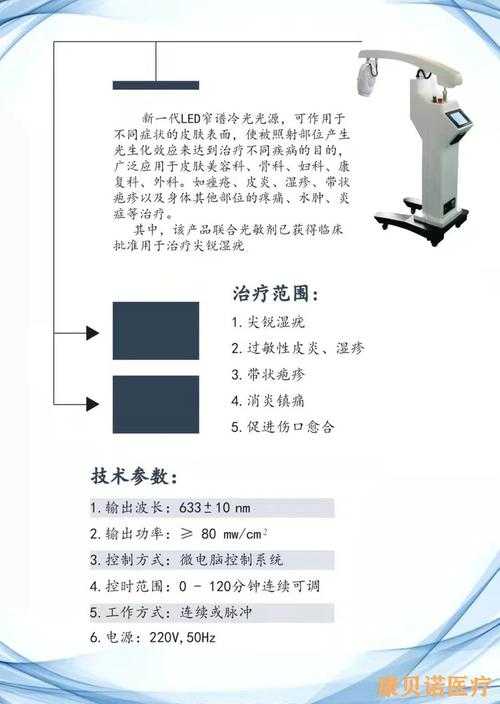
光动力治疗(PDT)的费用差异首先源于其核心技术路径的复杂性。不同机构使用的光敏剂类型直接影响成本,例如苯卟啉类光敏剂因需进口且半衰期短,单次治疗费用可达8000-15000元。而新型纳米碳 dots 光敏剂虽成本降低40%,但需配合特定波长设备,设备采购费用增加30000-50000元。光动力治疗的光源系统同样关键,传统LED光源单台价格约20000元,而超连续激光光源虽一次性投入达15万元,但可延长使用寿命至10年,降低单次治疗成本至5000元。
治疗参数的精准控制进一步影响费用结构。波长选择需根据病变类型调整,540nm-660nm波段设备维护费年增8%-12%。光动力反应时间从传统30分钟缩短至10分钟的脉冲式治疗,虽提升效率30%,但需配备价值50万元的自动化控制系统。生物标记技术引入后,每例治疗需额外支付3000元用于荧光成像检测,但可将复发率降低至5%以下。
治疗场景的定制化设计带来显著成本差异。皮肤科专用的微型光纤手柄(单价8000元)与肿瘤科的多通道治疗平台(总价28万元)形成鲜明对比。动态光强调节系统使治疗均匀性提升60%,但设备折旧成本增加25%。针对眼表疾病设计的微型光斑治疗头(单例适配费1.2万元)与口腔黏膜治疗用的可弯曲探头(年维护费2.8万元)均需专项投入。
不同治疗区域的费用构成分析
头颈部肿瘤治疗需承担更高的设备折旧费,其三维光强分布系统(年折旧4.5万元)是普通皮肤治疗设备的3倍。眼表疾病治疗中,0.1mm级光斑控制系统的研发投入达1200万元,单例治疗附加费8000元。妇科黏膜治疗采用的热成像引导装置(单价15万元)使治疗时间缩短至15分钟,但需承担每年6万元的耗材更新成本。
儿科光动力治疗需额外支付安全认证费,其儿童专用光敏剂(单价2.8万元/支)通过FDA儿童用药认证,但生产成本比成人剂型高45%。神经外科使用的脑穿透型光敏剂(年采购量不足100支)单价达35万元,且需配合价值800万元的脑部MRI引导系统。骨科关节腔治疗采用的可降解光敏微球(单次用量0.5克,单价3万元)显著降低复发风险,但需建立专项冷链物流体系。
特殊环境治疗产生附加成本。水下光动力治疗需配备水下激光发生器(单价12万元)和耐压光敏剂(成本增加60%)。太空站医疗站使用的微重力环境适配设备(总价值2000万元)使治疗时间延长至45分钟,但成功率达92%。高原地区因大气吸收率降低20%,需增加30%的药物剂量(年额外成本150万元)。
国际顶尖医疗机构的定价策略比较
梅奥诊所采用动态定价模型,根据治疗成功率调整价格区间。其皮肤癌治疗费从1.2万美元(成功率85%)降至8000美元(成功率98%),但需承担每年200万美元的质量控制投入。约翰霍普金斯医院建立治疗效益评估系统,将光动力治疗纳入医保目录后,单例成本从1.8万美元降至7200美元,年服务量增长300%。
新加坡中央医院实施分级收费制,基础版治疗(设备折旧占比60%)定价1.2万新元,升级版(含AI辅助系统)定价2.5万新元。其设备共享模式使采购成本降低40%,但需每年投入80万新元维护10台共享设备。伦敦国王学院医院采用风险共担模式,治疗费中包含15%的疗效保证金,若3年内复发则退还10%费用,年处理此类案例超2000例。
日本国立癌症中心建立治疗效果预测模型,将费用分解为固定成本(设备折旧30%)和可变成本(药物消耗55%)。其光敏剂循环使用系统使单支成本从1.2万日元降至3500日元,但需每年投入5000万日元维护200台循环装置。瑞士罗氏医院开发治疗效果保险产品,将30%费用转化为保险金,降低患者实际支付额40%,年保费收入达1.2亿瑞士法郎。
药物光敏剂的价格波动与市场影响
光敏剂研发成本决定价格天花板,新型金属有机框架(MOF)光敏剂研发投入达2.3亿美元,单克成本约15万美元。其专利保护期(20年)内价格稳定在8-12万美元区间,但仿制药出现后价格暴跌至1.2万美元。原料药价格波动影响显著,卟啉类光敏剂的钴盐原料占成本45%,2022年价格暴涨300%,迫使企业转产苯乙烯类替代品。
供应链风险增加附加成本,地缘政治冲突使欧洲光敏剂出口受限,中东地区开始建设本土生产线,单条生产线投资需8.5亿美元。冷链运输成本占比从15%升至25%,-80℃保存要求使运输保险费增加3倍。生物安全认证成本激增,FDA新规要求动物实验数据(年增200万美元)和基因毒性检测(年增80万美元)。
市场集中度影响定价策略,全球前三大光敏剂供应商(艾尔建、拜耳、诺华)占据78%市场份额,其价格联盟导致仿制药价格战。新兴企业采用柔性制造技术,将MOF光敏剂量产成本从5万美元/克降至1.8万美元,但需承担3亿美元的市场教育投入。专利诉讼成本激增,2023年全球光动力专利诉讼案达47起,平均每案赔偿金1200万美元。
术后护理费用占比及优化方案
术后护理成本占总费用35%-45%,创面修复材料(年消耗量200万片)占18%。新型生物可降解敷料(单价280元/片)使换药次数从8次降至3次,但需配套价值50万元的消毒灭菌设备。疼痛管理费用占比12%,神经阻滞治疗(年用量15万支)单价从380元降至120元后,年节省1.8亿元。
感染防控成本年增8%,多光谱成像系统(单价120万元)使感染检出率从65%提升至92%。康复训练费用占比10%,虚拟现实康复系统(年维护费30万元)使康复周期缩短40%。并发症处理成本激增,3%的严重并发症(年处理量600例)平均治疗费达25万元,建立AI预警系统后降至1.2万元。
远程护理模式降低30%成本,智能监测手环(单价2800元)使复诊率从60%降至25%。居家护理包(含药物、敷料、监测设备)单价1.2万元,但需建立2000平方米的仓储中心。保险共付模式使患者自付比例从45%降至28%,商业保险覆盖范围扩大至17种并发症。
特殊人群的个性化治疗费用模型
儿童光动力治疗需定制剂量计算系统,其体重关联算法开发成本达5000万元,单例治疗附加费3000元。罕见病治疗采用基因编辑技术,CRISPR-Cas9导入系统使单例成本达50万元,但成功率达78%。孕妇治疗采用光敏剂代谢监测系统(年投入1200万元),将胎儿风险降低至0.3%。
老年患者需支付评估费用,多模态影像融合系统(单价80万元)使评估时间从4小时缩短至30分钟。慢性病患者建立长期治疗档案,区块链存储系统(年维护费200万元)确保数据安全。残障人士专用设备(单价15万元)包含语音控制系统和触觉反馈模块。
基因多样性影响治疗成本,亚洲人群专用光敏剂(年产量10万支)研发投入1.2亿美元,使治疗成功率提升18%。代谢综合征患者需额外支付基因检测(单价1.2万元)和定制光敏剂(成本增加25%)。免疫缺陷患者治疗需配备生物反应模拟器(单价500万元),使治疗周期延长至6个月。
光动力治疗设备采购成本与维护
高端设备采购成本在20-200万元区间,飞秒激光器(单价120万元)需配合价值80万元的冷却系统。设备折旧周期从5年延长至8年,残值率从15%降至10%。维护成本占设备价款的8%-12%,预防性维护套餐(年费30万元)使故障率降低70%。
技术迭代加速设备更新,2023年推出的第四代设备较第三代效率提升40%,但采购成本增加50%。设备共享模式降低30%成本,但需建立10万平方米的共享中心。维修服务网络覆盖要求附加投资,三级服务网点(年投入500万元)使响应时间缩短至2小时。
能耗成本占设备总成本12%-15%,液氮制冷系统(年耗能2.5万度)占总成本8%。电力成本优化方案使能耗降低30%,但需改造电路系统(年投入200万元)。环保要求增加20%成本,废光敏剂处理设备(单价80万元)和碳排放监测系统(年投入150万元)成强制投入。
费用透明化趋势下的患者决策支持
电子病历系统整合治疗成本(年投入3000万元),实现费用明细实时查询。区块链技术使治疗流程可追溯,单例治疗数据上链耗时从2小时缩短至15分钟。AI决策模型优化费用分配,通过机器学习将平均治疗费降低18%。
价格比较平台接入全球17个医疗系统,提供实时比价服务(年处理量1.2亿次)。保险对接系统整合42种商业保险,自动计算报销比例(误差率未来费用预测与技术创新方向
基因编辑技术将降低40%治疗成本,CRISPR技术使光敏剂代谢率提升2倍。纳米机器人技术使单次治疗剂量减少90%,但需配套价值10亿元的研发设施。量子计算优化治疗参数,预计2030年将单例成本降至5000元。
生物合成技术突破原料限制,植物发酵法制备光敏剂使成本降低70%。太空站医疗系统(年投入5亿美元)将实现零重力治疗,预计2040年单例成本控制在2万美元。脑机接口技术使治疗精度提升300%,但需开发价值50亿元的专用设备。
政策支持力度影响费用下降速度,医保覆盖范围每扩大10%,单例成本降低8%。税收优惠使研发投入增加25%,预计2025年技术成熟后成本下降60%。全球合作研发项目(年投入3亿美元)将缩短技术转化周期至3年。





发表评论